自身免疫疾病是以局部或全身性异常炎症免疫反应为特征的炎症免疫性疾病,全球患者人群和药物规模都在增加,成为仅次于肿瘤的研发热门领域。其中,TNFα、JAK、IL-23和IL-6R等为自身免疫性疾病领域较为热门且成熟的靶点。近日,2026年1月5日,据中国国家药品监督管理局(NMPA)官网最新显示,千金药业控股子公司湖南千金湘江药业股份有限公司申报的巴瑞替尼片获批上市。资料显示,巴瑞替尼(Baricitini)是一种免疫系统用药,属于酪氨酸蛋白激酶(JAK)1/2抑制剂,主要用于治疗特应性皮炎、类风湿性关节炎和重度斑秃等相关疾病。


Janus激酶(JAK)是一种非受体型酪氨酸蛋白激酶,由七个同源结构域(JH)组成,包括JAK1-3和TYK2四个成员[2],其中JAK1、JAK3更多负责免疫调节,而JAK2主要与红细胞和血小板的生成相关。JAK激酶介导的JAK-STAT通路是人体最重要的炎症通路之一,与多项自身免疫性疾病的发病相关,如类风湿关节炎、银屑病和炎症性肠病等。巴瑞替尼作为是一种可逆的选择性非受体酪氨酸激酶1/2(JAK1/JAK2)抑制剂,是一种选择性免疫抑制药。巴瑞替尼通过选择性抑制JAK1和JAK2,阻断JAK-STAT信号通路,这是人体中关键的炎症信号传导途径之一,与多种自身免疫性疾病的发生发展密切相关。通过抑制这一途径,巴瑞替尼能够减轻炎症反应,并控制免疫系统的过度活跃。
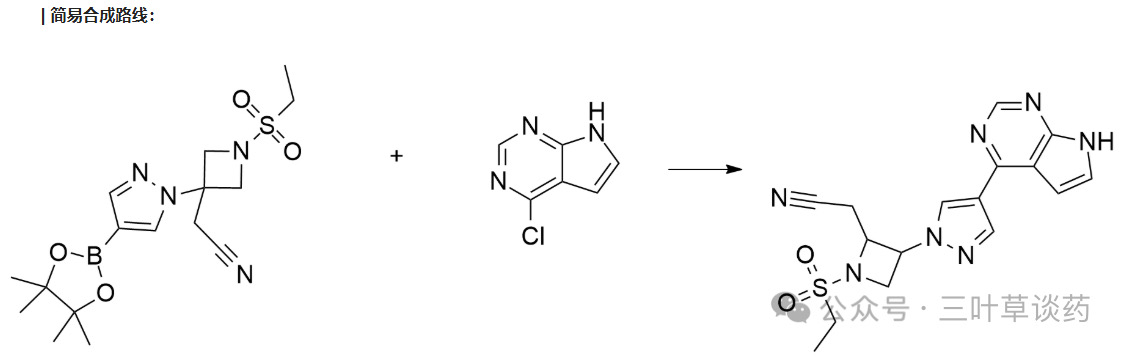
巴瑞替尼原研由礼来与Incyte公司联合开发,2017年2月,首次在欧盟和英国获批上市,适应症为治疗中度至重度活动性类风湿关节炎;2018年在美国FDA批准用于同类风湿关节炎适应症;2022年6月,FDA进一步批准其用于治疗成人重度斑秃,成为首款获批的口服斑秃疗法;此外,该药还获批了新型冠状病毒感染等适应症。在国内,巴瑞替尼于2019年7月在国内获批上市,用于治疗成人中重度活动性类风湿关节炎。2023年3月,巴瑞替尼斑秃适应症在中国获批。2023年10月,南京力博维制药研发的巴瑞替尼仿制药获批上市,成为首仿。截至目前为止,除原研外,国内已有复星万邦(江苏)医药、杭州朱养心药业、南京海纳制药、杭州民生药业、安徽泰恩康制药5家药企获得巴瑞替尼片生产批文。
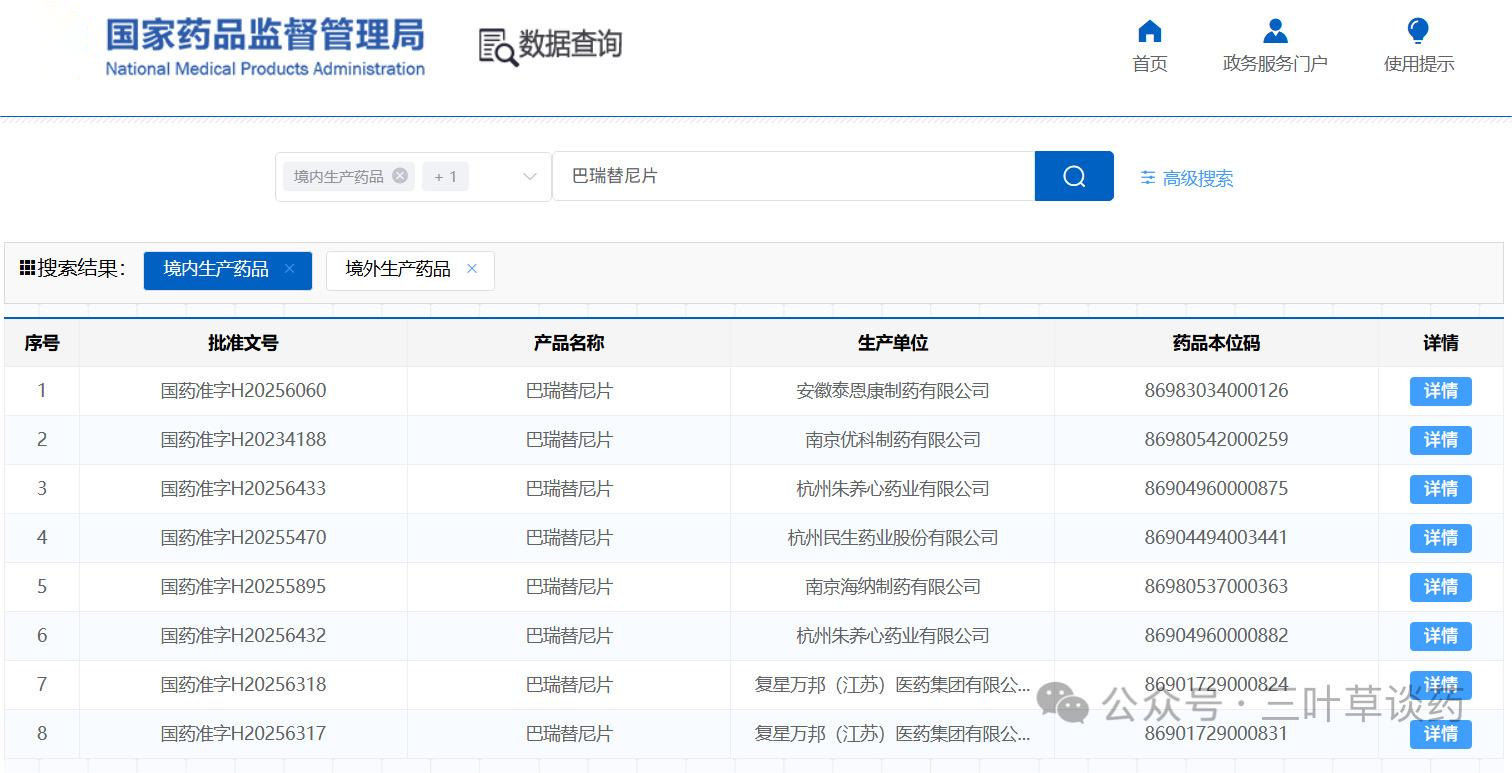
据相关数据统计显示,自上市以来,巴瑞替尼的销售额持续增长,2020年的全球销售业绩为6.38亿美元,同比增长50%;2021年为11.15亿美元,同比增长74.5%。然而,随着获批上市的JAK抑制剂增多,2022年巴瑞替尼销售额下滑至8.3亿美元。2022年6月,巴瑞替尼斑秃适应症获批,成为FDA批准的首个治疗斑秃的JAK抑制剂。2023年巴瑞替尼销售重回增长,达到9.23亿美元。
在国内市场,巴瑞替尼于2019年7月获批上市,并纳入2020版国家医保目录,适应症涵盖类风湿性关节炎与斑秃,同样展现出良好的市场前景。摩熵医药数据显示,巴瑞替尼当前院内总销量达8.29亿元,2023年销售额3.29亿元,同比暴增114.35%,2024年为2.52亿元。值得一提的是,巴瑞替尼核心中国化合物专利(CN200980116857.7)原应2029年3月10日到期,2024年1月29日被国知局宣告全部无效,请求人为南京斯帕克医药;其晶型专利(ZL201610136379.8)亦被国知局宣告全部无效,请求人为南京力博维制药。

巴瑞替尼核心专利被宣告全部无效后,仿制药大门已然敞开。若晶型专利亦被认定无效,其在国内的专利障碍或将彻底清除,这有望加速更多国产仿制药上市并推动价格下行,对仿制药企业及重度斑秃患者而言,无疑是重大利好。巴瑞替尼展现出强劲的市场增长潜力。目前,巴瑞替尼还在探索新的适应症,包括系统性红斑狼疮、溃疡性结肠炎、特应性皮炎和强直性脊柱炎等。随着这些新适应症的获批,巴瑞替尼的市场潜力有望进一步扩大。同时,随着国内药企对巴瑞替尼仿制药的进一步布局,必将为广大患者提供更多的治疗选择。
文章来源:三叶草谈药微信公众号
审核:王峰 郭江涛 石贵明
校对:小强




